เอนไซม์
คำนิยาม
เอนไซม์เป็นสารเคมีที่สามารถพบได้ทั่วร่างกาย พวกเขาตั้งปฏิกิริยาทางเคมีในการเคลื่อนไหวในร่างกาย
ประวัติศาสตร์
คำ เอนไซม์ มาจาก วิลเฮล์มฟรีดริชคูห์น 2421 และมาจากคำภาษากรีก enzymon ซึ่งหมายถึงยีสต์หรือ sourdough จากนั้นก็ค้นพบทางเข้าสู่วิทยาศาสตร์สากล สหภาพระหว่างประเทศของเคมีประยุกต์บริสุทธิ์ (IUPAC) และ International union of biochemstry (IUBMB) สร้างระบบการตั้งชื่อของเอนไซม์ซึ่งกำหนดตัวแทนของสารกลุ่มใหญ่นี้ว่าเป็นกลุ่มทั่วไป การตั้งชื่อซึ่งแบ่งประเภทของเอนไซม์ตามหน้าที่มีความสำคัญต่อการกำหนดงานของเอนไซม์แต่ละชนิด
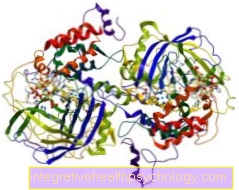
ภาพประกอบของเอนไซม์
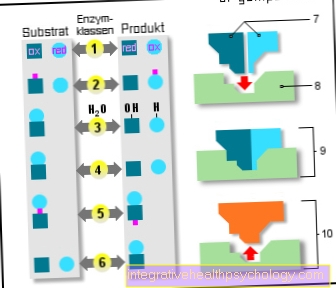
เอนไซม์
เอนไซม์ 6 คลาส:
- Oxidoreductases
(ออกซิเดชั่น / รีดิวซ์) - transferases
(การแพร่เชื้อ) - hydrolases
(การใช้น้ำ) - Lyases
(แตกแยก) - Isomerases
(สูตรโมเลกุลเดียวกัน) - ligases
(ปฏิกิริยาเพิ่มเติม) - พื้นผิว
- ศูนย์ที่ใช้งานอยู่
- เอนไซม์ / สารตั้งต้น
ซับซ้อน - เอนไซม์ / ผลิตภัณฑ์
ซับซ้อน
ภาพรวมของทั้งหมดรูปภาพของเขาโดย Dr-Gumpert สามารถพบได้ที่: ภาพประกอบทางการแพทย์
การตั้งชื่อ
การตั้งชื่อ เอนไซม์เปิดอยู่ หลักการพื้นฐานสามประการ ซึ่งเป็นรากฐาน.ชื่อเอนไซม์ที่ลงท้ายด้วย -ase อธิบายถึงเอนไซม์หลายชนิดในระบบ ชื่อเอนไซม์นั้นอธิบายถึงปฏิกิริยาที่เอนไซม์กำหนดให้เคลื่อนที่ (เร่งปฏิกิริยา) ชื่อเอนไซม์ยังเป็นการจำแนกประเภทของเอนไซม์ นอกจากนี้ระบบรหัสที่ ระบบหมายเลข ECซึ่งเอนไซม์ถูกสร้างขึ้นภายใต้รหัสตัวเลข ตัวเลขสี่ตัว สามารถพบได้ ตัวเลขแรกระบุระดับเอนไซม์ รายชื่อเอนไซม์ที่ตรวจพบทั้งหมดช่วยให้มั่นใจได้ว่าสามารถค้นหารหัสเอนไซม์ที่ระบุได้เร็วขึ้น แม้ว่ารหัสจะขึ้นอยู่กับคุณสมบัติของปฏิกิริยาที่เอนไซม์เร่งปฏิกิริยา แต่ในทางปฏิบัติรหัสตัวเลขพิสูจน์แล้วว่าไม่สามารถทำได้ ชื่อที่เป็นระบบตามกฎข้างต้นถูกใช้บ่อยขึ้น ปัญหาเกี่ยวกับระบบการตั้งชื่อเกิดขึ้นเช่นกับเอนไซม์ที่กระตุ้นปฏิกิริยาต่างๆ ดังนั้นบางครั้งจึงมีหลายชื่อ เอนไซม์บางชนิดมีชื่อที่ไม่สำคัญซึ่งไม่ได้บ่งชี้ว่าสารที่กล่าวถึงเป็นเอนไซม์ เนื่องจากชื่อนี้ถูกใช้กันอย่างแพร่หลายบางส่วนจึงถูกเก็บรักษาไว้
การจำแนกตามการทำงานของเอนไซม์
จากข้อมูลของ IUPAC และ IUBMB เอนไซม์แบ่งออกเป็นเอนไซม์ 6 ประเภทตามปฏิกิริยาที่เริ่มต้น:
- Oxidoreductases
Oxidoreductases ตั้งค่าปฏิกิริยารีดอกซ์ในการเคลื่อนที่ ในปฏิกิริยาเคมีนี้อิเล็กตรอนจะผ่านจากคู่ปฏิกิริยาหนึ่งไปยังอีกคู่หนึ่ง มีการปลดปล่อยอิเล็กตรอน (ออกซิเดชั่น) ของสารหนึ่งและการดูดซับอิเล็กตรอน (รีดักชัน) โดยสารอื่น
สูตรสำหรับปฏิกิริยาที่เร่งปฏิกิริยาคือ A ?? + B? A? + B?
สาร A ปล่อยอิเล็กตรอน (?) และถูกออกซิไดซ์ในขณะที่สาร B ดูดซับอิเล็กตรอนนี้และถูกลดจำนวนลง นี่คือสาเหตุที่ปฏิกิริยารีดอกซ์เรียกอีกอย่างว่าปฏิกิริยารีดักชัน - ออกซิเดชั่น
ปฏิกิริยาการเผาผลาญหลายอย่างเป็นปฏิกิริยารีดอกซ์ ออกซิเจนจะถ่ายเทออกซิเจนอย่างน้อยหนึ่งอะตอมไปยังสารตั้งต้น - transferases
Transferases จะถ่ายโอนกลุ่มฟังก์ชันจากวัสดุพิมพ์หนึ่งไปยังอีกวัสดุหนึ่ง หมู่ฟังก์ชันคือกลุ่มอะตอมในสารประกอบอินทรีย์ที่กำหนดคุณสมบัติของสารและพฤติกรรมการเกิดปฏิกิริยาในระดับมาก สารประกอบทางเคมีที่มีหมู่ฟังก์ชันเดียวกันจะถูกจัดกลุ่มเป็นชั้นของสารเนื่องจากคุณสมบัติที่คล้ายคลึงกัน กลุ่มการทำงานจะถูกแบ่งออกตามว่าพวกเขาต่างกันหรือไม่ เฮเทอโรอะตอมเป็นอะตอมภายในสารประกอบอินทรีย์ที่ไม่ใช่คาร์บอนหรือไฮโดรเจน
เช่น -OH -> กลุ่มไฮดรอกซิล (แอลกอฮอล์) - hydrolases
ไฮโดรเลสแยกพันธะในปฏิกิริยาย้อนกลับโดยใช้น้ำ เอสเทอร์เอสเทอร์เปปไทด์ไกลโคไซด์กรดแอนไฮไดรด์หรือพันธะ C-C ปฏิกิริยาสมดุลคือ A-B + H2O? A-H + B-OH.
เอนไซม์ที่อยู่ในกลุ่มของไฮโดรเลส ได้แก่ อัลฟากาแลคโตซิเดส - Lyases
Lyases ซึ่งเรียกอีกอย่างว่า synthases กระตุ้นความแตกแยกของผลิตภัณฑ์ที่ซับซ้อนจากพื้นผิวที่เรียบง่ายโดยไม่ต้องแยก ATP ออก รูปแบบปฏิกิริยาคือ A-B → A + B
ATP คืออะดีโนซีนไตรฟอสเฟตและนิวคลีโอไทด์ซึ่งประกอบด้วยไตรฟอสเฟตของอะดีโนซีนของนิวคลีโอไซด์ (และเป็นส่วนประกอบของกรดนิวคลีอิกที่อุดมด้วยพลังงาน) อย่างไรก็ตาม ATP ส่วนใหญ่เป็นรูปแบบสากลของพลังงานที่ใช้ได้ทันทีในทุกเซลล์และในขณะเดียวกันก็เป็นตัวควบคุมที่สำคัญของกระบวนการจัดหาพลังงาน หากจำเป็น ATP จะถูกสังเคราะห์ใหม่จากแหล่งเก็บพลังงานอื่น ๆ (ครีเอทีนฟอสเฟตไกลโคเจนกรดไขมัน) โมเลกุลของ ATP ประกอบด้วยกากอะดีนีนน้ำตาลไรโบสและฟอสเฟตสามตัว (? ถึง?) ในเอสเทอร์ (?) หรือพันธะแอนไฮไดรด์ (? และ?) - Isomerases
ไอโซเมอร์เร่งการแปลงทางเคมีของไอโซเมอร์ Isomerism คือการเกิดสารประกอบทางเคมีสองชนิดขึ้นไปที่มีอะตอมเดียวกัน (สูตรเชิงประจักษ์เดียวกัน) และน้ำหนักโมเลกุลซึ่งแตกต่างกันในการเชื่อมต่อหรือการจัดเรียงเชิงพื้นที่ของอะตอม สารประกอบที่เกี่ยวข้องเรียกว่าไอโซเมอร์
ไอโซเมอร์เหล่านี้แตกต่างกันในทางเคมีหรือ / และทางกายภาพและมักจะมีคุณสมบัติทางชีวเคมีด้วย Isomerism ส่วนใหญ่เกิดขึ้นกับสารประกอบอินทรีย์ แต่ยังรวมถึงสารประกอบโคออร์ดิเนชัน (อนินทรีย์) ไอโซเมอริซึมแบ่งออกเป็นพื้นที่ต่างๆ - ligases
Ligases เร่งการก่อตัวของสารที่มีความซับซ้อนทางเคมีมากกว่าสารตั้งต้นที่ใช้ แต่ในทางตรงกันข้ามกับไลเอสจะมีฤทธิ์ทางเอนไซม์กับ ATP cleavage เท่านั้น การสร้างสารเหล่านี้จึงต้องใช้พลังงานที่ได้จากการแตกตัวของ ATP
เอนไซม์บางชนิดสามารถกระตุ้นปฏิกิริยาหลายอย่างบางครั้งก็แตกต่างกันมาก หากเป็นกรณีนี้พวกมันจะถูกกำหนดให้กับคลาสเอนไซม์หลายตัว
คุณอาจสนใจบทความเหล่านี้:
- Alpha-glucosidase
- เอนไซม์ไลเปส
- trypsin
การจำแนกตามโครงสร้างของเอนไซม์
เอนไซม์เกือบทั้งหมดเป็นโปรตีนและสามารถจำแนกได้ตามความยาวของห่วงโซ่โปรตีน:
- โมโนเมอร์
เอนไซม์ที่ประกอบด้วยห่วงโซ่โปรตีนเพียงเส้นเดียว - oligomers
เอนไซม์ที่ประกอบด้วยโซ่โปรตีนหลายตัว (โมโนเมอร์) - โซ่หลายเอนไซม์
เอนไซม์รวมหลายชนิดที่ทำงานร่วมกันและควบคุมซึ่งกันและกัน โซ่ของเอนไซม์เหล่านี้กระตุ้นให้เกิดขั้นตอนต่อเนื่องในการเผาผลาญของเซลล์
นอกจากนี้ยังมีโซ่โปรตีนแต่ละชนิดที่มีกิจกรรมของเอนไซม์หลายชนิดเรียกว่าเอนไซม์มัลติฟังก์ชั่น
การจำแนกตามปัจจัยร่วม
การจำแนกประเภทอื่นคือการจัดหมวดหมู่ตามการพิจารณาปัจจัยร่วม ปัจจัยร่วมโคเอนไซม์และสารตั้งต้นเป็นชื่อของการจำแนกประเภทต่างๆของสารที่มีอิทธิพลต่อปฏิกิริยาทางชีวเคมีผ่านการมีปฏิสัมพันธ์กับเอนไซม์
โมเลกุลและไอออนอินทรีย์ (ส่วนใหญ่เป็นไอออนของโลหะ)
เอนไซม์โปรตีนบริสุทธิ์ประกอบด้วยโปรตีนโดยเฉพาะและศูนย์กลางที่ใช้งานนั้นเกิดขึ้นจากกากกรดอะมิโนและกระดูกสันหลังของเปปไทด์เท่านั้น กรดอะมิโนเป็นกลุ่มของสารประกอบอินทรีย์ที่มีหมู่คาร์บอกซี (-COOH) อย่างน้อยหนึ่งกลุ่มและกลุ่มอะมิโนหนึ่งกลุ่ม (-NH2)
โฮโลเอนไซม์ประกอบด้วยส่วนประกอบของโปรตีนเอโพเอนไซม์และปัจจัยร่วมซึ่งเป็นโมเลกุลที่มีน้ำหนักโมเลกุลต่ำ (ไม่ใช่โปรตีน) ทั้งสองอย่างรวมกันมีความสำคัญต่อการทำงานของเอนไซม์
โคเอนไซม์
โมเลกุลอินทรีย์เป็นปัจจัยร่วมเรียกว่าโคเอนไซม์ หากโควาเลนต์ผูกพันกับเอโพเอนไซม์จะเรียกว่ากลุ่มเทียมหรือสารตั้งต้นร่วม กลุ่มขาเทียมเป็นคำที่ใช้อธิบายส่วนประกอบที่ไม่ใช่โปรตีนอย่างแน่นหนา (โดยปกติจะเป็นโควาเลนต์) ที่เชื่อมโยงกับโปรตีนที่มีฤทธิ์เร่งปฏิกิริยา
Cosubstrates เป็นชื่อของการจำแนกประเภทต่างๆของสารที่มีอิทธิพลต่อปฏิกิริยาทางชีวเคมีผ่านการมีปฏิสัมพันธ์กับเอนไซม์ ในฐานะที่เป็นตัวเร่งปฏิกิริยาทางชีวภาพโมเลกุลจะเร่งปฏิกิริยาในสิ่งมีชีวิตเอนไซม์จะเร่งปฏิกิริยาทางชีวเคมี พวกเขาลดพลังงานกระตุ้นที่ต้องเอาชนะเพื่อให้สามารถเปลี่ยนสารได้